 |
:: Информация :: |  |
||
|
|
||||
 |
 |
|||
| :: Популярные статьи :: |
|
Синдром раздраженной толстой кишки при дисбактериозе кишечника Синдром недостаточности пищеварения при дисбактериозе кишечника |
 |
Современные представления о грибковой патологии пищеварительного тракта
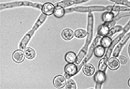
С. А. Бурова, доктор медицинских наук, профессор
Национальная академия микологии, ГКБ № 81, Москва
В гастроэнтерологии, как и в других областях медицины, динамично развиваются методы диагностики и лечения грибковых инфекций на основе изучения физиологии, микробиологии, фармакологии, молекулярной патологии и медицинской генетики. Детально изучаются уже известные варианты болезни и описываются редкие и новые нозологические формы.
Грибы, являясь нормальными комменсалами желудочно-кишечного тракта (ЖКТ), становятся патогенными при определенных условиях. Это касается в основном дрожжеподобных грибов Candida spp., виды и даже штаммы которых различаются по факторам агрессии, способности к адгезии и инвазии [15].
Candida albicans — наиболее частый возбудитель кандидоза ЖКТ. Однако в последние годы большую роль играют Candida non-albicans (C. krusei, C. tropicalis, C. kefyr, C. glabrata, C. parapsilosis); у лиц с иммунодефицитом их пропорция составляет более 50%, при «относительно нормальном» иммунитете — 15%.
Грибы Candida (условно-патогенные микроорганизмы) заселяют ЖКТ — этот феномен называется колонизацией, — процесс протекает бессимптомно. Исследование взрослых здоровых добровольцев показало, что Candida albicans присутствует в орофарингеальной зоне у 20–30% из них, в тонком кишечнике — у 50–54%, в толстом кишечнике — у 55–70% и в фекалиях — у 65–70% [9, 13]. При исследовании состава микрофлоры полости рта у населения нескольких стран Европы обнаружено присутствие грибов у 10–25% людей, в кале — у 65–80% [11, 17]. Детально изучена колонизация зева грибами Candida у больных гемобластозами: она составила 33% [8]. В биоптатах гастродуоденальных язв в 17–30% случаев находят дрожжеподобные грибы [12]. У 50% жителей Германии в микробиоте кишечника присутствуют грибы, а у онкогематологических больных колонизация кишечника составляет 63–65% [10, 11]. Нельзя забывать, что у 0,8–4% пациентов грибы случайно обнаруживаются в пузырной и протоковой желчи, а при желчнокаменной болезни — у 15–20%.
Бессимптомное пребывание грибов в ЖКТ может прекратиться, когда они приобретают патогенные свойства. Так, у больных с нейтропенией грибы из кишечника могут диссеминировать в печень, селезенку и легкие, а в катетер-ассоциированной ситуации грибы попадают непосредственно в ток крови, достигают сердца и почек.
Дрожжеподобный гриб Cryptococcus neoformans в патологии ЖКТ как этиологический фактор играет незначительную роль. Он чаще поражает нервную систему и, диссеминируя из первичного очага, вовлекает гастроинтестинальный тракт. Описаны единичные случаи (чаще посмертно) криптококкового эзофагита, стоматита, терминального илеита, колита, холецистита, панкреатита. Как правило, они относились к ВИЧ-серопозитивным больным, а также к пациентам, страдающим гипергаммаглобулинемией Е с рецидивирующими абсцессами печени и перианальной зоны.
Болезни ЖКТ, вызванные диморфными патогенными грибами (II группы патогенности), зарегистрированы в Южной Америке, но время от времени встречаются как спорадические случаи по всему миру. Большинство диморфных грибов в природе существуют в мицелиальной форме, попав в организм они трансформируются в дрожжеподобные и приобретают патогенные свойства. Пероральный путь проникновения не характерен, в ЖКТ эти грибы попадают при диссеминации из других органов. Blastomyces dermatitidis продуцирует гранулематозное повреждение в желудке и тонком кишечнике. Coccidioides immitis, Histoplasma capsulatum, Paracoccidioides brasiliensis и Sporothrix schenckii поражают кишечник только при диссеминации из кожных очагов и респираторного тракта [6, 15].
Грибы Aspergillus spp. редко вызывают болезнь ЖКТ, только в случаях стойкой нейтропении, кахексии и при других отягощающих состояниях.
Грибы класса Zygomycetes могут привести к развитию интестинального зигомикоза, который, как правило, ассоциирован с амебиазом, голоданием, диабетическим кетоацидозом, почечным гемодиализом. Penicillium spp. и Geotrichum поражают ЖКТ также редко.
Дрожжеподобные, плесневые и некоторые диморфные грибы — это условно-патогенные, оппортунистические микроорганизмы, которые широко распространены в окружающей среде и легко могут попадать на кожу, слизистые оболочки полости рта, гениталий и в дыхательные пути. Кроме того, для грибов характерен эндогенный способ существования (миконосительство).
ЖКТ покрыт слизистой оболочкой, состоящей из двух компонентов — поверхностного скользкого, слизистого слоя, по которому микроорганизмы легко продвигаются вдоль всего ЖКТ, и более глубокого плотного гликопротеинового слоя с остатками сиаловой кислоты, который формирует физиологический барьер. Адгезия и последующая инвазия грибов через этот плотный слой возможны только благодаря продукции грибами протеолитических «ферментов инвазии»: коагулазы, каталазы, козеиназы, фосфолипазы, а также фибриллярных протеиновых комплексов и эндотоксинов [15].
При физиологическом благополучии между макро- и микроорганизмами существует определенное равновесие, в котором играют роль, с одной стороны, факторы устойчивости организма к микроскопическим грибам, а с другой — факторы патогенности грибов.
Устойчивость организма зависит от принадлежности к группам риска и состояния иммунной системы.
Перечислим факторы риска развития грибковых инфекций ЖКТ.
Поражение слизистых оболочек полости рта (красный плоский лишай, зубные протезы, травмы, ксеростомия, использование гормональных ингаляторов).
Хронические заболевания ЖКТ (атрофический гастрит, гипоацидность желудка, ахалазия, бульбит, эрозивно-язвенные заболевания пищевода и кишечника, дивертикулез, полипоз, гастроэзофагальная рефлюксная болезнь, энтероколит, болезнь Крона, синдром раздраженной кишки, обсемененность желудка Helicobacter pylori, дисбиоз, микст-инфекция кишки).
Травмирование слизистой оболочки (ожоги, пищеводно-желудочный зонд, эндотрахеальная интубация).
Беременность.
Период новорожденности (недоношенность, массивность инфекции при прохождении через родовые пути, естественное несовершенство иммунной системы).
Пожилой возраст (старение иммунной системы, сопутствующие заболевания, уменьшение амплитуды продольных сокращений пищевода, силы сокращений сфинктеров, нарушение процессов всасывания и т. д.).
Онкологические и гематологические заболевания (нейтропения).
Эндокринопатии (особенно сахарный диабет).
СПИД, ВИЧ-инфицированность.
Трансплантационные операции.
Состояния, требующие пребывания в отделениях интенсивной терапии.
Тяжелые аллергические заболевания.
Прием антибиотиков, цитостатиков, гормонов и других химиопрепаратов в неадекватных дозах.
Нарушения питания, в том числе голодание с целью снижения веса.
Алкоголизм, курение, наркомания.
Важным компонентом защиты от инвазии ЖКТ является иммунная система, ассоциированная с кишечником. Клеточная часть этой системы включает в себя интраэпителиальные лимфоциты, которые препятствуют дисперсии возбудителя через lamina propria и агрегации в пейеровых бляшках. В-лимфоциты кишечника участвуют в продукции секреторных IgA и IgM, которые уменьшают способность грибов к адгезии.
Т-клетки здорового организма продуцируют защитный интерферон, усиливают фагоцитоз, активируют Т-цитотоксические лимфоциты. СД4 и СД8 укрепляют местный иммунитет в ЖКТ. Причем оказалось, что цитотоксичность СД8 играет более существенную роль в предотвращении заболевания, чем предполагали раньше.
В защите важны также макрофагальный и нейтрофильный фагоцитоз, препятствующие диссеминации грибковой, особенно кандидозной инфекции.
У ВИЧ-пациентов и больных с нейтропенией, у которых фагоцитоз резко подавлен, местная инвазия и диссеминация инфекции наступают очень быстро. Известно, что нейтрофилы хотя и не могут полностью защитить слизистую оболочку ЖКТ от «атаки» грибов, но благодаря собственной «киллерной» субстанции через специфический механизм запускают активацию комплемента, который усиливает фагоцитоз. Следует отметить, что фагоцитоз особенно важен при кандидозной инфекции, но «не работает» в тканях против капсулированных криптококков и большинства мицелиальных грибов.
Нормальные биохимические, гистохимические и физиологические процессы в ЖКТ, своевременная регенерация эпителиоцитов, кислотно-ферментативный барьер, полноценная перистальтическая активность также являются защитными факторами, которые препятствуют проникновению грибковой и бактериальной флоры [4]. Роль желудочной кислоты в предотвращении внедрения грибов в слизистую неоспорима. В среде с пониженной кислотностью грибы Candida приобретают патогенные свойства, появляются вегетирующие формы, образуется псевдомицелий или мицелий, повреждающий слизистую оболочку. У ВИЧ-инфицированных лиц, для которых характерна ахлоргидрия, попадающие с пищей грибы Candida могут вызывать кандидоз желудка, в то время как у людей с нормальным иммунитетом эта локализация встречается редко. Роль кислотности желудочного сока в развитии бактериальной и грибковой инфекции кишечника не подтверждена.
Облигатные микроорганизмы желудка и кишечника (аэробные лактобациллы, анаэробные бифидум-бактерии, нормальная кишечная палочка и др.) также играют защитную роль. Применение антибиотиков убивает, наряду с патогенными, и эти «полезные» бактерии, открывая на слизистой оболочке рецепторы адгезии для грибов [2].
Нельзя не упомянуть также о Helicobacter pylori, который довольно часто обитает в желудке, вызывает гастрит, язвенную болезнь, а иногда оказывает канцерогенное воздействие. В свою очередь, лечение хеликобактериоза антибиотиками приводит к активации грибов Candida и кандидозу желудка [1]. Ассоциации грибов с Helicobacter pylori и другими бактериями в ЖКТ встречаются нередко, что требует продуманного адекватного подхода к тактике лечения.
В желудке могут также присутствовать Saccharomyces cerevisiae и некоторые виды Candida, способные сбраживать и ферментировать до винного спирта сахара, попадающие с пищей в желудок. Этот феномен называется синдромом «пивоваренного завода» [14].
Вирулентность грибов, патогенные факторы, как и полисахариды (маннаны), плазмокоагулаза, эндотоксины, липиды, глюкоконъюгаты, влияют на развитие заболевания. Даже от внутривидовых способностей грибов зависит, разовьются ли в каждом конкретном случае кандиданосительство или болезнь [13]. Например, серотип В Candida albicans считается более вирулентным и наиболее распространенным возбудителем орофарингеального кандидоза у ВИЧ-инфицированных больных, также он поражает генитоуринарную систему и нередко выделяется из зева у гомосексуалистов.
Микроскопически факторы агрессии грибов Candida проявляются формированием ростковых трубок, псевдогифов и истинного мицелия — за счет них грибы могут врастать в стенку фагоцитов. Однако дрожжи, которые не способны продуцировать мицелий, такие, как Candida glabrata, Cryptococcus neoformans, также могут вызывать заболевания ЖКТ.
Диагностика
Тщательное изучение анамнеза, выявление факторов риска, хронических заболеваний ЖКТ, патогномоничных клинических симптомов играют большую роль в своевременности установления диагноза.
В последние годы за счет эндоскопических технологий расширились возможности диагностики грибкового эзофагита и гастрита. При эзофагогастродуоденоскопии обращают внимание на гиперемию и изъязвления слизистой, наличие белых налетов и «пленок», сужение просвета пищевода, скопление слизи. Во время этой процедуры в обязательном порядке следует брать материал для микробиологического исследования, так как не всегда этиология этих проявлений грибковая. Причем информативность исследования налетов выше, чем биоптатов (95% по сравнению с 39%).
Особенно перспективны видеоинформационные эндоскопические исследования с цифровой регистрацией и анализом изображения. Четкое разграничение неизмененных и патологических тканей, анализ гистохимических процессов в слизистой оболочке пищеварительного тракта возможны с помощью эндоскопической спектроскопии и флюоресцентной эндоскопии. Видео- и колоноскопия, хромоэндоскопия на фоне «лекарственного» сна по технологии «Диантек» имеют высокое качество исследования, безболезненность манипуляций и отсутствие стресса и страха у пациентов.
Следует, однако, подчеркнуть, что инвазивные манипуляции при воспаленной слизистой ЖКТ небезопасны, могут способствовать грибковой и бактериальной диссеминации, а иногда приводят к травме и перфорации стенки пищевода или желудка. Эндоскопическая ультрасонография с допплеровским картированием, контрастным усилением тканевых и сосудистых структур перспективна, она позволяет детально дифференцировать все слои стенки пищеварительного тракта. Неинвазивные методы — виртуальная эндоскопия, позволяющая получить трехмерное изображение, магнитно-резонансное исследование — имеют большое будущее [3].
Изучение гастродуоденальной моторики с помощью сцинтиграфии и электрогастрографии также важно для диагностики и назначения дополнительных лекарственных средств, так как нарушение двигательной функции желудка, «застой» в ЖКТ создают условия для размножения грибов и бактерий. Колоноскопия дает возможность оценить состояние слизистой кишечника, наличие белого налета, язвенных дефектов и т. д. В перспективе в гастроэнтерологии будут внедряться методы, в основе которых лежат новые научно-практические исследования: иммуноферментный анализ фекальных антигенов, ПЦР и даже генетическое тестирование [3].
Еще одним достаточно информативным методом в гастроэнтерологии является рентгенография пищевода, желудка и кишечника. Она дает возможность выявить дефекты наполнения (депо бария), изъязвления, деформацию, конвергенцию складок, изменения контуров и глубины перистальтики, сужение или расширение пищеводной трубки. С помощью рентгенографии желудка можно оценить его моторику, своевременность эвакуации пищевого комка, что важно для понимания патогенеза заболевания.
Лабораторное подтверждение грибкового заболевания ЖКТ возможно при микроскопировании и/или культуральном исследовании смывов со слизистых оболочек полости рта и пищевода, содержимого желудка и кишечника, патологических «пленок», налетов и др. Количественная оценка грибов в биосубстратах должна проводиться в сопоставлении с клинической симптоматикой, с учетом наличия фоновых заболеваний, микст-инфекции и т. д. Например, обнаружение на слизистых единичных колоний Candida не является основанием для постановки диагноза «кандидоз» у иммунокомпетентных пациентов.
В кале диагностическую значимость приобретает количество колоний (более 105–106). По-другому, с более низким диагностическим порогом, интерпретируются результаты посевов у иммуносупрессированных лиц, при нейтропении у больных СПИДом и в отделениях интенсивной терапии. Следует также обращать внимание на способность грибов к вегетации и образованию мицелия, так как это является одним из лабораторных признаков, подтверждающих диагноз кандидоза.
Гистологическое (окраска по Гомори–Гроккоту, ШИК-реакция) и цитологическое (окраска по Романовскому–Гимзе) исследования биоптатов позволяют обнаружить тканевые формы грибов. Многими авторами эти методы рассматриваются как наиболее достоверные. Кроме того, мицелий и псевдомицелий в тканях служат подтверждением наличия инвазивной формы грибковой инфекции ЖКТ.
Кандидоз
Это наиболее распространенная грибковая оппортунистическая висцеральная патология. Агрессивные свойства грибов Candidа проявляются в их способности через стадию адгезии и инвазии поражать слизистые оболочки любых органов, в том числе и ЖКТ. Причем «атаке» подвергается чаще всего многослойный плоский эпителий полости рта и пищевода, реже — однослойный цилиндрический эпителий кишечника. Поэтому, как правило, в верхних отделах ЖКТ происходит инвазия грибов Candidа, а в отделах, расположенных ниже желудка, — колонизация. В то же время в кишечнике даже на стадии адгезии могут наблюдаться клинические симптомы — проявления неинвазивного кандидоза [10].
Язвенные дефекты пищевода, желудка и кишечника поддерживают грибковую колонизацию вплоть до инвазии. Желудочно-кишечный кандидоз нередко приводит к кандидемии.
Классификация кандидоза
I. Орофарингеальный кандидоз.
Кандидоз полости рта у новорожденных.
Псевдомембранозный кандидоз.
Атрофический кандидоз полости рта (чаще у пожилых).
Эритематозный кандидоз (новая форма).
Срединный ромбовидный глоссит.
Лейкоплакия, ассоциированная с кандидозом.
Ангулярный кандидозный хейлит.
Кандидозный гингивит (изолированно встречается редко).
II. Кандидозный эзофагит.
Без эрозий.
С эрозиями.
III. Кандидоз желудка.
Эрозивно-фибринозный гастрит (диффузный).
Вторичный кандидоз на фоне язвенной болезни.
IV. Кандидоз кишечника.
Псевдомембранозный.
Коллагеновый.
Лимфоцитарный.
V. Кандидозный проктосигмоидит.
VI. Перианальный кандидоз.
VII. Секреторная диарея, ассоциированная с кандидозом.
Среди всех локализаций кандидоза пищеварительного тракта орофарингеальная занимает 1-е место.
О кандидозе полости рта упоминал еще Гиппократ, а впервые описал его хирург Лангенберк в 1839 г.
Кандидозный стоматит у новорожденных — распространенное заболевание. В первые дни после рождения слизистые ребенка устойчивы к грибам.
В дальнейшем недостаточная секреция IgA и постепенное снижение антимикробного иммунитета, переданного от матери, приводят к высокой заболеваемости. Патогномоничный синдром — белые творожистые налеты на слизистой полости рта, так называемая «молочница» [16].
Кандидоз ассоциирован также с ношением протезов. При этом развивается атрофический кандидоз, огромное количество грибов скапливается в щечных складках на фоне красного точечного воспаления слизистой; инвазия, как правило, отсутствует.
Кандидозный эзофагит в стационарах общего профиля встречается у 1,3–2,8% больных, в отделениях трансплантации — до 4%, при диссеминированном карциноматозе — от 2,8 до 6,7%. Это заболевание протекает часто без субъективных жалоб и выявляется случайно при «сплошных» исследованиях населения в 1–7% случаев [5, 17]. Иногда больные отмечают боль и дискомфорт при прохождении твердой и жидкой пищи, дисфагию, гиперсаливацию. По глубине поражения эндоскопически выделяют четыре типа — от легкого отека, гиперемии, единичных белых налетов < 1 мм в диаметре до массивного воспаления, деформации и кровоточивости слизистой, изъязвлений, вплоть до перфорации.
Кандидоз желудка, как правило, развивается вторично на фоне язвенной и гастроэзофагальной рефлюксной болезни. Ахлоргидрия, в свою очередь, способствует колонизации грибов на слизистой, с последующей инвазией, особенно в зонах дефекта (язвы, эрозии), что замедляет репарацию, появляется болевой синдром, иногда отмечается кровоточивость язвы.
Кандидозное поражение кишечника обычно проявляется абдоминальным дискомфортом, диареей, вздутием живота, болевым синдромом и другими симптомами. Изучение микробиоценоза кишечника позволяет конкретизировать аморфный «энтероколит», а именно дифференцировать псевдомембранозный колит, вызываемый Clostridium difficile, острый процесс в кишечнике, вызываемый ротовирусами и Escherichia coli, от кандидоза или дисбактериоза с преимущественным кандидозным компонентом.
Грибковому поражению билиарной системы способствуют предшествующие дискинезия желчевыводящих путей, диспанкреатизм, лямблиоз, холестаз, гипотония желчного пузыря и другие поражения. При этих состояниях создаются благоприятные условия для размножения грибов и других микроорганизмов. Причиной кандидозного холецистита могут быть камни желчных протоков, которые часто являются «резервуаром» грибов, некоторые авторы даже называют их «грибковыми тельцами» или «кандидозными камнями».
Микозы желчевыводящих путей встречаются чаще, чем принято считать. Микробиологическое исследование порций желчи, полученных при многофракционном дуоденальном зондировании, позволяет дифференцировать грибковую от бактериальной или функциональной патологии двенадцатиперстной кишки, желчного пузыря, желчевыводящих путей и печени.
Лечение
Лечение кандидоза пищеварительного тракта, как, впрочем, и других грибковых инфекций, должно быть комплексным и этиопатогенетическим.
При появлении жалоб со стороны ЖКТ больному прежде всего следует соблюдать строгую диету и отказаться от вредных привычек.
Необходимо принимать средства, направленные на устранение факторов, предрасполагающих к развитию кандидоза, проводить коррекцию сопутствующих заболеваний.
При подозрении на кандидоз, развившийся на фоне неспецифического язвенного колита, болезни Крона, хронического воспаления стенки кишки подбирают глюкокортикостероиды с минимальным системным действием и "мягкие" иммуномодуляторы.
Лечение язвенной и гастроэзофагальной рефлюксной болезни проводят антисекреторными препаратами производными бензимидазола - ингибиторами протонной помпы париетальных клеток (нексиум, париет, ланзап); а также блокаторами гистаминовых H2-рецепторов (квамател, ульфамид, ульцеран, гастросидин, фамосан).
С целью предотвращения заброса содержимого желудка в пищевод повышают тонус нижнего пищеводного сфинктера и двигательную активность ЖКТ, назначая современные препараты - антагонисты серотониновых 5-НТ4-рецепторов.
Функциональное заболевание "синдром раздраженной кишки" лечат аналогами соматостатина, каппа-антагонистами.
Антихеликобактерную терапию омепразолом, амоксициллином, тинидазолом и др. проводят с большой осторожностью, так как Helicobacter pylori часто существует в ассоциации с грибами Candida spp., а последние на фоне антибиотикотерапии резко активизируются.
Необходима противогрибковая терапия. Список противогрибковых средств с каждым годом пополняется новыми эффективными препаратами. Среди современных антимикотиков выделяют несколько групп.
Полиены: амфотерицин В (амфоглюкамин), липидный комплекс Амфо В (амфолип), липосомальный Амфо В (амбизом), коллоидная дисперсия Амфо В (амфоцил).
Триазолы: флуконазол (дифлюкан), вориконазол (вифенд), равуконазол (в стадии клинических испытаний), итраконазол (орунгал), позаконазол (в стадии клинических испытаний), альбаконазол (в стадии клинических испытаний).
Аллиламины: тербинафин (ламизил).
Эхинокандины: каспофунгин (кансидас), микафунгин, анидулафунгин (в стадии клинических испытаний).
Многолетние наблюдения, проводившиеся на базе Центра глубоких микозов и посвященные эффективности лечения грибковых заболеваний пищеварительного тракта (более 150 больных), позволяют нам выделить из общего ряда препаратов наиболее эффективное адекватное этиотропное средство. Это антимикотик из группы триазолов — флуконазол (дифлюкан, дифлазон, флюкостат), использующийся при лечении дрожжеподобных инфекций ЖКТ (кандидоз, криптококкоз). Он обладает высочайшей эффективностью, которая основана на угнетении системы цитохрома Р-450 и последующем нарушении синтеза эргостерола в клеточной мембране дрожжеподобного гриба. За счет высокой биодоступности, активной всасываемости в ЖКТ, отсутствия влияния на синтез тестостерона и кортизола, флуконазол хорошо переносится и не вызывает побочных воздействий. Препарат обладает уникальной способностью проникать через гематоэнцефалический барьер, что особенно важно в случае диссеминации грибковой инфекции из ЖКТ в кровь и ЦНС.
При назначении per os объем всасывания флуконазола в пищеварительной системе составляет более 90%, причем степень его резорбции высока даже при ахлоргидрии, что выгодно отличает этот триазол от полиенов и других азолов. Препарат не оказывает негативного влияния на процессы всасывания в кишечнике при совместном приеме с антацидами. Наивысшая концентрация препарата в плазме при приеме его внутрь или внутривенно достигается через 0,5–1,5 ч. В то же время период полувыведения длительный — 30 ч, а процент связывания с белками плазмы низкий — 11–12%. Отсутствие токсических действий флуконазола объясняется не только слабым связыванием с белками, но и большим объемом (79,6%) выведения его через почки с мочой в неизмененном виде.
В настоящее время на российском рынке флуконазол представлен 18 генерическими копиями, которые имеют аналогичные фармакокинетические характеристики, хорошо переносятся больными. Однако в отношении клинической и микологической эффективности некоторые из них несколько уступают оригинальному флуконазолу — дифлюкану.
Флуконазол выпускается в трех формах:
раствор по 50, 100 и 200 мл во флаконе для внутривенного применения (2 мг/мл);
капсулы желатиновые по 50, 100, 150 и 200 мг;
порошок во флаконе для приготовления 60 мл суспензии с апельсиновым вкусом для приема внутрь (50 мг/5 мл).
Нами разработаны комплексные схемы лечения кандидоза пищеварительного тракта с учетом локализации, глубины поражения, состояния иммунозащитных сил, наличия отягощающих заболеваний. Этиотропное значение в этой схеме отводилось флуконазолу, который назначали взрослым по 2–2,5 мг/кг, в среднем 100–150 мг в сутки, 2–3 нед. В первый день доза удваивалась.
Детские дозировки: для новорожденных — 7–12 мг/кг в сутки; для детей дошкольного и школьного возраста 50–100 мг/сут; курс лечения составлял 7–14 дней.
Таким образом, как показала наша практика, при системных микозах, в том числе и при кандидозе ЖКТ, раствор флуконазола для внутривенного введения и суспензия применяются чаще, чем капсулы.
Причины развития патологии пищеварительной системы многообразны, клиническая симптоматика вариабельна. Грибковые инфекции, вызываемые дрожжеподобными, плесневыми и диморфными грибами, составляют 8–10% от общего числа заболеваний ЖКТ, а колонизированы грибами до 80% населения. Заболеванию особенно подвержены ВИЧ-инфицированные и больные с нейтропенией. Для диагностики используют современные эндоскопические и рентгенологические методы. Проводят микробиологическое исследование биосубстратов для выяснения этиологии заболевания. Наиболее распространенная грибковая инфекция ЖКТ — кандидоз. Схема лечения грибковой патологии пищеварительного тракта включает назначение эффективного, нетоксичного антимикотика, противовоспалительных, общеукрепляющих и иммуномодулирующих средств. Терапия должна проводиться на фоне диеты, больные нуждаются в диспансерном наблюдении.
По материалам: medlinks.ru
21/11/2012









